OPTIMAL研究:《肿瘤学年鉴》重磅发表!口服紫杉醇为HER2阴性晚期乳腺癌患者迎来便利新选择
2026-03-20
前言
2026年3月13日,肿瘤学领域顶刊《肿瘤学年鉴》(Annals of Oncology,IF=65.4)在线发表了紫杉醇口服溶液(DHP107,Liporaxel®)的关键III期临床试验OPTIMAL的研究结果1。在中国大陆地区,这项国际多中心III期临床试验由中国医学科学院肿瘤医院徐兵河院士牵头,联合国内19家研究中心参与。该研究在复发/转移阶段未接受过化疗的HER2阴性复发或转移性乳腺癌患者中,首次证实了一种全新的口服紫杉醇方案,其疗效不劣于当前标准的静脉紫杉醇方案,为临床带来了兼具疗效、安全性与便利性的治疗新选择。

研究背景
紫杉醇作为乳腺癌甚至更多实体瘤治疗的基石药物,其注射剂型临床应用已逾20年。但静脉给药导致的超敏反应、神经毒性及频繁住院等问题长期困扰医患2,严重影响患者的生活质量的同时,也增加了就医时间成本与医疗负担。因此,开发一种安全、有效且更加便捷的口服紫杉醇方案,成为了临床亟待满足的需求。
紫杉醇口服溶液(DHL107,Liporaxel®)正是在此背景下诞生的创新口服紫杉醇制剂,通过创新性脂质自乳化递药技术成功攻克紫杉醇口服吸收的难题,使患者在家即可完成治疗。作为全球首个获批上市的口服紫杉醇制剂,DHL107在中国胃癌III期注册临床研究中,证实其中位生存期(mOS)延长了2.59个月(HR 0.770, 95.5% CI: 0.635, 0.934, p=0.006),优于紫杉醇注射液,无进展生存期(PFS)不劣于紫杉醇注射液,且安全性可控3。OPTIMAL研究则旨在进一步验证DHP107在晚期乳腺癌患者中的疗效和安全性。
研究设计
OPTIMAL研究是一项国际、多中心、开放标签、非劣效、随机对照的III期临床试验,旨在评估DHP107相较于紫杉醇注射液在HER2阴性复发或转移性乳腺癌患者中的疗效与安全性。研究共纳入549例来自韩国、中国及欧洲51个研究中心、复发/转移阶段既往未接受过化疗的复发或转移性乳腺癌患者,1:1随机分配接受紫杉醇口服溶液DHP107(200 mg/ m² ,每日两次口服,第1、8、15天给药)或紫杉醇注射液(80 mg/ m² ,静脉注射,第1、8、15天给药),每28天为一个治疗周期。
主要终点为研究者评估的无进展生存期(PFS,PP集),非劣效性界值预设为1.33(即若紫杉醇口服溶液组相较于紫杉醇注射液组PFS的HR值95%置信区间上限小于1.33,即认为达到预期的非劣效统计学推断)。次要终点包括独立中心评估的PFS 、总生存期(OS)、治疗失败时间(TTF)、客观缓解率(ORR)、疾病控制率(DCR)、生活质量(QoL)和安全性。
研究结果
两组患者的基线特征均衡可比。在所有随机人群中,中国患者占比达52.8%。中位随访时间为39个月。
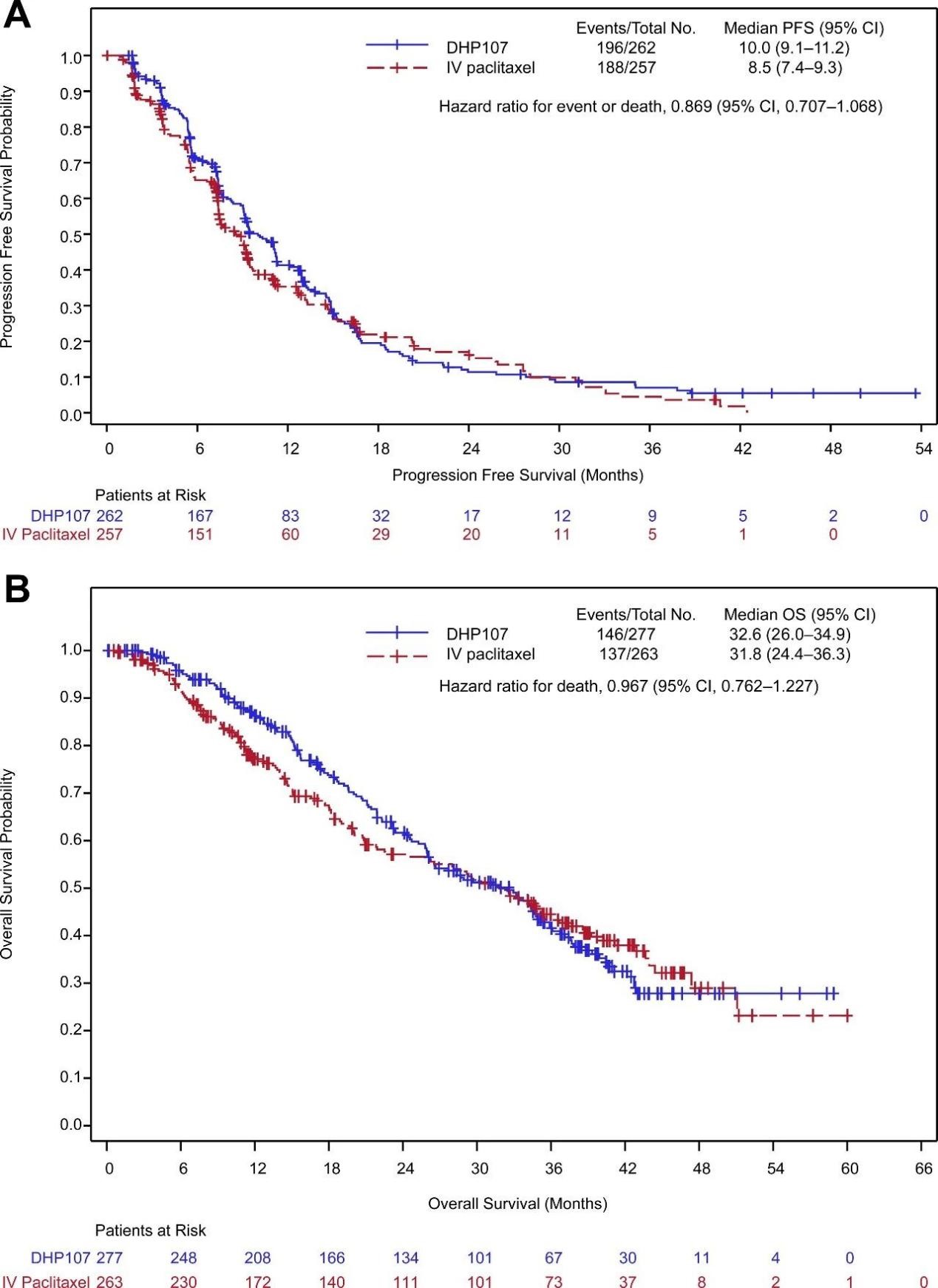
研究达到主要终点:紫杉醇口服溶液组的中位无进展生存期(mPFS)为10.0个月,紫杉醇注射液组为8.5个月(HR=0.869; 95%CI,[0.707–1.068),上限 < 1.33非劣效界值),这意味着紫杉醇口服溶液可减少13.1%的进展或死亡风险。
紫杉醇口服溶液和紫杉醇注射液的中位总生存期(mOS)相当,分别为32.6月 vs 31.8个月(HR=0.967;95%CI, 0.762-1.227)。
在其他次要终点方面,紫杉醇口服溶液组均显示出数值上的优势趋势:
中位TTF:7.6个月 vs. 7.4个月(HR=0.875;95% CI, 0.731–1.046)
ORR:43.3% vs. 38.8%
DCR:89.2% vs. 84.4%
在安全性方面,两组治疗期间不良事件发生率接近(97.8% vs 96.6%);紫杉醇口服溶液组无治疗相关死亡;紫杉醇注射液组发生 1 例(0.4%)治疗相关死亡。
与静脉方案相比,紫杉醇口服溶液展现出了不同的安全性特征:紫杉醇口服溶液组血液学毒性和胃肠道反应较高,但整体安全可控。但外周神经病变发生率更低(37.9% vs. 48.3%),超敏反应发生率也更低(0.7% vs. 2.7%),且无需为预防过敏而进行预处理。
在生活质量方面,两组患者在治疗期间的生活质量评分相当且保持稳定。
结论与展望
OPTIMAL研究证实,在HER2阴性复发或转移性乳腺癌患者中,紫杉醇口服溶液DHP107的疗效非劣效于紫杉醇注射液方案,且安全性可控。DHP107作为首个在乳腺癌III期研究中证实疗效的口服紫杉醇制剂,有望将治疗场景从“医院输注”向“居家口服”转变,显著减少患者往返医院的频次、输液等待时间及相关交通与陪护成本,从而提升治疗体验与生活质量,为临床提供了一种疗效确切、安全可控且具有居家给药便利性的一线化疗新选择。
目前,紫杉醇口服溶液胃癌适应症已在中国获批,乳腺癌适应症中国上市申请已获受理。未来,随着更多靶向药和免疫检查点抑制剂的口服或皮下制剂走上市场,与化疗口服药物组合形成便捷方案,将进一步推动更多瘤种向“慢病化”管理演进,为更多患者带来持续的临床获益。
1. Xu B, Jeong H, Sun T, et al. OPTIMAL: A Multinational Phase III Study of Oral Paclitaxel (DHP107) versus Intravenous Weekly Paclitaxel in HER2-Negative Recurrent or Metastatic Breast Cancer. Ann Oncol. Published online March 13, 2026.
2. 紫杉醇制剂超敏反应预处理指导意见专家组.紫杉醇制剂超敏反应预处理指导意见[J].中国现代药学,2019,36(8):1023-1027.
3. Jin Li, Mingzhu Huang, Ting Deng, et al. Paclitaxel oral solution versus paclitaxel injection as second-line therapy in advanced gastric cancer: A randomized, open-label, non-inferiority phase 3 trial. Journal of Clinical Oncology. 2024, 42: 405. 2016;doi:10.1001/jamaoncol.2016.4188.
关于三生制药
三生制药是一家集研发、生产和销售为一体的生物制药领军企业,致力于以高品质的药品提高患者生存质量,为人类健康造福。目前,公司拥有190余项国家发明专利授权,40余种上市产品,30余种在研产品,覆盖肾科、肿瘤科、自身免疫性疾病、眼科及皮肤科等多种治疗领域。公司拥有包括抗体药物国家工程研究中心以及生物药和化药双平台在内的6大研发基地,4大生产基地及4大CDMO基地。未来,三生制药将继续秉持“珍爱生命、关注生存、创造生活”的理念,全力打造全球领先的中国生物制药企业。请访问www.3sbio.com获取更多信息。
警示说明及前瞻性陈述
本新闻稿包含前瞻性陈述,例如涉及业务和产品前景,或公司的意图、计划、认知、预期及策略。该等前瞻性陈述是根据本公司现有的资料,并按本新闻稿发布时的展望陈述。该等前瞻性陈述基于若干预测、假设及前提,其中一些是主观性的或不受我们控制。该等前瞻性陈述可能被证明是不正确的,或将来可能无法实现。就任何新产品或产品的新适应症, 我们无法确保其将能成功开发或最终上市销售。该等前瞻性陈述受各种风险及不明朗因素影响。我们的其他公开披露文件可能提供该等风险及不明朗因素的更多信息。所涉及之科学信息可能只是初步的和研究性的。本公司股东及潜在投资者在买卖本公司股份时,请务必谨慎行事。